В настоящее время новостные ленты информационных агентств всего мира пестрят сообщениям об эпидемии коронавируса, изначально вспыхнувшей в Китайской Народной Республике и уже охватывающей другие, особенно близлежащие, страны. Общее число заразившихся коронавирусом 2019-nCoV перевалило за миллион, количество смертельных случаев насчитывает десятки тысяч [1, 2].
Агентство Bloomberg привело списки погибших от вируса с указанием симптомов, пола, возраста на 23 января 2020 г [3]. Преимущественно, летальный исход наблюдается у пожилых мужчин старше 60 лет. Наиболее частые симптомы – лихорадка, кашель и затрудненное дыхание. Развитие заболевания может привести к прогрессирующей дыхательной недостаточности из-за повреждения альвеол и даже смерти. Клинические врачи определяли заболевание как вирусно-индуцированную пневмонию в соответствии с клиническими симптомами и другими критериями, включая повышение температуры тела, снижение лимфоцитов и лейкоцитов, новые легочные инфильтраты при рентгенографии грудной клетки и отсутствие очевидного улучшения при лечении антибиотиками в течение трех дней.
Вирус стремительно распространяется по миру. На 28 января 2020 года подтвержденные случаи заражения по странам [2] (по ссылке находится постоянно обновляемая интерактивная карта с новыми случаями заражений и смертей, возможны сбои из-за большой нагрузки): Материковый Китай – 4409, Гонконг – 8, Таиланд – 8, Макао – 6, Австралия – 5, Тайвань – 5, США – 5, Япония – 4, Малайзия – 4, Сингапур – 5, Южная Корея – 4, Франция – 3, Германия – 1, Вьетнам – 2, Камбоджа – 1, Канада – 1, Непал – 1, Шри-Ланка – 1. В России пока не выявлено ни одного подтвержденного случая заражения. Скорость роста числа зараженных на территории материкового Китая соответствует экспоненциальной зависимости. В Китае проводятся карантинные мероприятия, введен запрет на поездки в некоторые пострадавшие районы, по сути, изолировав миллионы людей [3]. Всемирная организация здравоохранения в четверг заявила, что вспышка еще не стала глобальной чрезвычайной ситуацией, но ВОЗ внимательно следит за ситуацией.
Инфекционным агентом является вирус 2019-nCoV (Wuhan coronavirus, Wuhan seafood market pneumonia virus) – новый штамм коронавируса, выявленный в декабре 2019 года во время вспышки пневмонии в Ухане (Wuhan, КНР) [4]. 2019-nCoV способен передаваться от человека к человеку. Пока не ясно, насколько легко это происходит, но обычно человеческие коронавирусы распространяются по воздуху при кашле и чихании. Инкубационный период составляет до 14 дней, в течение которого также возможно заражение от человека к человеку. В середине января геном вируса 2019-nCoV уже был расшифрован и внесен в базу данных [5]. 2019-nCoV представляет собой одноцепочечный РНК-содержащий вирус, РНК-последовательность которого состоит из 29903 нуклеотидов. Из-за сообщений о том, что первоначальные случаи имели эпидемиологические связи с крупным рынком морепродуктов и животных, считается, что вирус имеет зоонозное происхождение, хотя это не было подтверждено. Сравнение генетических последовательностей между этим вирусом и другими существующими образцами вируса показало 79,5 %-ное сходство с SARS-CoV и 96 %-ное с коронавирусом летучих мышей (BatCoV RaTG13, ранее обнаруженный у азиатского подковоноса, Rhinolophus affinis) [6], с вероятным происхождением от летучих мышей. Название SARS-CoV (severe acute respiratory syndrome-related coronavirus) расшифровывается как «коронавирус, относящийся к тяжёлому острому респираторному синдрому». Уже установлено, что новый вирус 2019-nCoV использует тот же рецептор проникновения в клетку, ACE2, что и SARS-CoV [6].
В целом, коронавирусы (СoV) – это группа вирусов, вызывающих заболевания у млекопитающих и птиц. У людей СoV вызывают респираторные инфекции, которые обычно являются легкими, но в редких случаях могут быть смертельными. У коров и свиней они могут вызывать диарею, а у цыплят – заболевание верхних дыхательных путей. К настоящему времени еще нет ни вакцин, ни противовирусных препаратов, которые были бы одобрены для профилактики или лечения заболеваний, вызванных СoV. По классификации, коронавирусы являются вирусами подсемейства Orthocoronavirinae в семействе Coronaviridae, отряда Nidovirales. Коронавирусы представляют собой оболочечные вирусы с положительно-полярным одноцепочечным РНК-геномом ((+)ssRNA) и с нуклеокапсидом спиральной симметрии. Размер генома СoV составляет примерно от 26 до 32 килобаз и является самым большим среди РНК-вирусов.
Коронавирусы были обнаружены в 1960-х годах; самыми ранними из них были обнаружены вирус инфекционного бронхита у кур и два вируса из носовых полостей пациентов с простудой, которые впоследствии были названы человеческим коронавирусом 229E и человеческим коронавирусом OC43. С тех пор были идентифицированы другие члены этого семейства, в том числе SARS-CoV в 2003 году, HCoV NL63 в 2004 году, HKU1 в 2005 году, MERS-CoV в 2012 году и 2019-nCoV в 2019 году; большинство из них были связаны с серьезными инфекциями дыхательных путей [7].
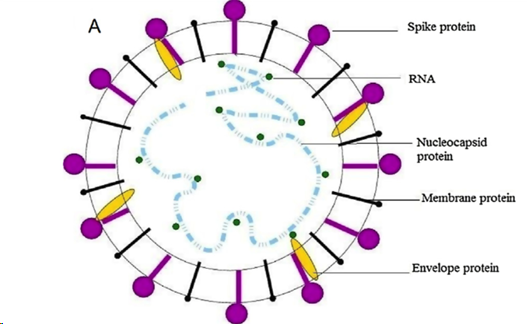
Бета-коронавирусы, к которым относится BatCoV RaTG13, близкородственный к новому вирусу 2019-nCoV, являются одним из четырех родов коронавирусов. В более ранней литературе этот род также известен как коронавирусы 2-й группы.
Среди Бета-CoV наибольшее клиническое значение для людей имеют штаммы OC43 и HKU1 линии A, SARS-CoV и 2019-nCov линии B, и MERS-CoV линии C. MERS-CoV является первым бета-коронавирусом, принадлежащим к линии С, который поражает людей [8]. Альфа- и бета-коронавирусы происходят из генного пула летучих мышей [9, 10].
За последние два десятилетия коронавирусы вызвали две крупномасштабные пандемии: SARS и MERS (ближневосточный респираторный синдром) [11, 12].
SARS – коронавирус, вызвавший эпидемию тяжёлого острого респираторного синдрома (ТОРС, атипичная пневмония) в 2002 году, начавшуюся в Китае. В процессе размножения SARS разрушает клетки лёгочных альвеол, что может вести к смерти. Было подтверждено 8098–8422 случаев заражения, в результате чего в 17 странах зарегистрировано 774 летальных исходов (смертность 9,6–11 %) [13, 14].
Ближневосточный респираторный синдром (Middle East respiratory syndrome, MERS, MERS-CoV) вызывается бета-коронавирусом. Вспышка эпидемии наблюдалась преимущественно в странах Ближнего Востока в 2012 году; у большинства пациентов развивалось тяжелое острое респираторное заболевание, требующее госпитализации, и уровень смертности составлял 30–60 % [15]. Всего пострадало около 2000 человек. Сам вирус был выделен из летучей мыши [16]. MERS-CoV тесно связан с коронавирусами летучей мыши Tylonycteris HKU4 и Pipistrellus HKU5 – генетические последовательности идентичны более чем на 90 % [17].
По состоянию на март 2017 года ВОЗ сообщила о 1905 подтвержденных случаях MERS, включая 677 случаев смерти в 27 странах. MERS распространяется среди людей, вызывая серьезные осложнения, которые приводят к смерти; Отсюда вытекает необходимость разработки эффективных лечебно-профилактических средств. Было показано, что вспышка MERS в больнице произошла из-за передачи вируса от человека человеку [18]. В настоящее время не существует зарегистрированного лечения или вакцины против этой болезни, но инфекция MERS-CoV скорее управляется режимом медикаментозного лечения, в дополнение к некоторым профилактическим мерам для избегания повторного заражения [19]. Несколько исследований показали, что различные терапевтические средства могут ингибировать репликацию MERS-CoV в клеточной культуре.
В 2018 году был опубликован обширный обзор современных вариантов лечения ближневосточного респираторного синдрома (MERS) и роли пептидов как потенциальных терапевтических компонентов [20]. В этом обзоре кратко описаны важные лекарственные мишени MERS-CoV, представлены терапевтические варианты, доступные для лечения MERS, и описана их эффективность, а также обсуждается роль исследований пептидов в вирусологии и важность антимикробных пептидов (AMP) в качестве потенциальных терапевтических агентов по отношению к MERS. Предполагается, что быстрое развитие подходов вычислительной биологии может быть разработана новая и эффективная терапия MERS с использованием AMP.
Структурные и неструктурные белки MERS-CoV как лекарственные мишени
Путь передачи MERS-CoV от животных к человеку не был однозначно определен [21], но передача могла происходить от летучих мышей [16] через верблюдов, служащих промежуточными хозяевами [22]. Было показано, что MERS-CoV модулирует врожденный иммунный ответ, выработку антигена, митоген-активируемую протеинкиназу (MAPK) и апоптоз.
Структура MERS-CoV состоит из четырех структурных белков, включая белковый шиловидный отросток (S), белок оболочки (E), белок мембраны (M) и белок нуклеокапсида (N). Белок S представляет собой трансмембранный гликопротеин типа I, который находится на поверхности вирусной оболочки в состоянии тримера. Он состоит из субъединиц S1 и S2 и играет роль в проникновении вируса, связывании и слиянии. Субъединица S1 имеет рецептор-связывающий домен (RBD). RBD отвечает за связывание с клеточным рецептором дипептидилпептидазы 4 (DPP4). Субъединица S2 включает в себя две области, а именно гептадные повторы 1 и 2 (HR1 и HR2), которые собираются в комплекс, называемый ядро слияния, и представляет собой ключевую архитектуру мембранного синтеза [23]. Белок Е имеет общую длину 82 аминокислотных остатка и присутствует в основном во внутриклеточных мембранах вируса и играет основную роль в сборке вируса, почковании и внутриклеточном транспорте [24]. Белок М является компонентом вирусной оболочки, который играет роль в морфогенезе и сборке вируса посредством его взаимодействия с другими вирусными белками [25]. Белки S, M и E встраиваются в мембрану эндоплазматическиого ретикулума и транспортируются в область комплекса Гольджи, в которой они взаимодействуют с белками N с образованием частиц [26]. Это взаимодействие, в конечном итоге, будет мешать слиянию клеточных и вирусных мембран. Таким образом, перечисленные пептиды могут иметь большое значение в терапии с использованием пептидов. Кроме того, MERS-CoV состоит из двух больших полипротеинов, а именно pp1a и pp1ab, которые затем расщепляются на 16 неструктурных белков (nsps) [27]. Две протеазы, папаин-подобная протеаза (PLpro или nsp3) и 3C-подобная протеаза (3CLpro или nsp5), ответственны за обработку всех 16 nsps, которые необходимы для репликации и транскрипции. PLpro отвечает за расщепление в позиции 1-3 для развития трех nsps, тогда как 3CLpro расщепляет оставшиеся позиции 4-16. Эти nsps ответственны за вирусную РНК-зависимую активность РНК-полимеразы (nsp12), активность ДНК-праймазы (nsp8), активность РНК-геликазы (nsp13), активность экзорибонуклеазы (nsp14), активность эндорибонуклеазы (nsp15) и активность 2′-O-метилтрансферазы ( nsp16) [28]. Активность 2′-O-метилтрансферазы стимулируется nsp10, который действует как аллостерический активатор nsp16. Исследования показывают, что nsps коронавируса можно использовать в качестве мишеней для разработки новых методов лечения (см. ссылки в обзоре [20]). Как структурные, так и неструктурные белки могут выступать в качестве терапевтических мишеней, в которых могут быть реализованы различные терапевтические варианты, и они будут обсуждаться далее.
Роль пептидов как потенциальных противовирусных / противокоронавирусных агентов
Существует интерес к пептидным лекарственным средствам и их миметикам в качестве потенциальных антагонистов различных патогенов. Изучение пептидов является важным аспектом фармацевтических исследований, и в настоящее время в клинических испытаниях оценивается приблизительно 140 пептидных препаратов [29].
Причины использования пептидов заключаются в том, что (i) они ингибируют белок-белковые взаимодействия; (ii) их можно использовать в качестве альтернативной терапии заболеваний, на которые трудно воздействовать; (iii) существуют передовые методы для увеличения периода полужизни пептида и (iv) у них более короткое время выхода на рынок [30]. Пептидные лекарственные средства зачастую имеют незначительные побочные эффекты и хорошую переносимость по сравнению с химическими лекарственными средствами. Между тем, специфичность лечения высока. Пептидные препараты нуждаются в особых условиях хранения, в противном случае функция белка становится неактивной, что приводит к низкой пероральной биодоступности и склонности к быстрому метаболизму.
Многие пептидные ингибиторы проявляют активность против вирусов [31-33] и др. ссылки в обзоре [20]. Например, пептид RVFV-6, полученный из проксимального участка ствола мембраны гликопротеина Gc RVFV, предотвращает слияние вируса при лихорадки Рифт-Валли. Он также проявляет активность против неродственных вирусов, таких как EBOV и VSV. Производное пептида яда скорпиона Kn2-7 было идентифицировано как потенциальный агент против ВИЧ-1 с низкими цитотоксическими эффектами.
Отсутствие эффективного лечения способствовало разработке дополнительных терапевтических агентов с повышенной эффективностью для преодоления побочных эффектов, возникающих при современном лечении MERS. В последнее десятилетие наблюдается растущий интерес к области пептидной терапии из-за многочисленных побочных эффектов химических препаратов [34].
AMP являются превосходными кандидатами в качестве новых терапевтических агентов, поскольку, как сообщалось, они обладают анти-коронавирусной активностью [35]. AMP являются компонентами первой линии защиты иммунной системы, вырабатываемой как эукариотическими, так и прокариотическими видами. Это небольшие положительно заряженные пептиды, которые обладают избирательной токсичностью в отношении грамположительных и грамотрицательных бактерий, простейших, грибов и вирусов [36-39]. Их селективная токсичность обусловлена тем, что мембранный бислой микробов богат липополисахаридами и липотейхоевой кислотой, поэтому он заряжен отрицательно в отличие от положительного заряда AMP [38]. Противовирусные AMP имеют несколько способов действия, включая блокирование проникновения вируса при взаимодействии гепарансульфата, ингибирование проникновения вируса путем слияния со специфическими клеточными рецепторами и прекращение слияния вируса путем взаимодействия с гликопротеинами, мембраной и оболочкой вируса [40].
Ниже приведена таблица 1, в которой показаны (А) пептиды, ингибирующие слияние вируса; (B) пептиды, ингибирующие репликацию вируса; (C) пептиды, ингибирующие проникновение вируса. Подробное описание доступно по ссылкам, приведенным в таблице.
Часть данных в таблице 1 получена авторами [20] из база данных по антимикробным пептидам (APD, Antimicrobial Peptide Database – http://aps.unmc.edu/AP/), которая является оригинальной базой данных, работающей онлайн с 2003 года. В базе содержится и постоянно добавляется информация по пептидам, обнаруженным в разнообразных организмах. На сегодняшний день в ней содержится 3160 записей, в которые включено 139 защитных пептидов человека, 305 – млекопитающих, 1087 активных пептидов земноводных (1018 от лягушек), 134 пептида рыб, 45 пептидов рептилий, 42 – птиц, 559 – членистоногих, [310 – насекомых, 69 – ракообразных, 7 – многоножек , 171 – хелицерных, (43 от пауков, 88 от скорпионов)], 45 – моллюсков, 6 AMP от простейших и ряд синтетических пептидов. База позволяет выполнять поиск по названию организма, пептида, аминокислотной последовательности, по биологической активности и тд. Также предусмотрен модуль предсказания параметров пептида по аминокислотной последовательности и модуль дизайна антимикробных пептидов. Небезынтересен статистический раздел базы, суммирующий собранную информацию.
Заключение
Существует острая необходимость в разработке наиболее эффективной терапии коронавирусов, таких как MERS, 2019-nCoV и новых, еще неизвестных, потенциально опасных агентов. Также необходима разработка протоколов для использования в рандомизированных контролируемых исследованиях. Исследования показали, что пептиды превратились в высокоэффективные агенты для передачи сигнала при вирусных заболеваниях. Предполагается, что противомикробные пептиды могут быть успешным терапевтическим вариантом для нового возбудителя MERS. Вычислительная биология в сочетании с вирусологией с большей эффективностью может ускорить наиболее продвинутый путь разработки пептидной терапии против MERS-CoV. Кроме того, предполагается, что переориентация существующих и клинически одобренных анти-коронавирусных и антивирусных пептидных препаратов может быть использована в качестве многообещающего направления для разработки новых агентов против MERS-CoV и подобных коронавирусов.




