1. Актуальность исследования
1.1. Перспективы применения пептидов в качестве хондропротекторов
Хрящевая ткань представляет собой один из видов соединительной ткани, основным структурным элементом которой являются хондроциты, расположенные в межклеточном матриксе. Матрикс представлен рыхлыми волокнами соединительной ткани, образованными из гликозаминогликанов; также в его состав входят коллаген 2-го типа и гиалуроновая кислота. Последние два компонента вырабатываются хондроцитами путем ряда биохимических реакций, для успешного осуществления которых необходимы витамины, микроэлементы, ферменты, энергия, а также составляющие гликозаминогликанов, среди которых главную роль играют сульфаты глюкозамина, хондроитина и кератана. Гликозаминогликаны, соединенные при помощи белковых связей образуют еще более крупные структуры – протеогликаны, выполняющие роль амортизаторов, полностью восстанавливающие свою форму после механического сдавления.
Если процессы катаболизма активных компонентов матрикса преобладают над процессами синтеза, структура хрящевой ткани нарушается, снижается подвижность сустава (Алексеева Л.И., 2012). Кроме того, в таком суставе увеличивается продукция веществ, инициирующих процессы воспаления: циклооксигеназы, цитокинов (в частности, интерлейкина-1в). Такие процессы, приводящие в дегенеративным изменениям в хрящевой поверхности суставов, характерны для людей пожилого возраста, а также для лиц молодого и среднего возраста, имеющих в течение длительного времени тяжелые физические нагрузки (например, при занятиях спортом или в профессиональной деятельности).
На фоне приема традиционно применяемых хондропротекторов могут развиться различные побочные эффекты. В связи с этим поиск новых препаратов-хондропротекторов на основе пептидов, эффективных и не имеющих побочных эффектов, является актуальной задачей современной медицины.
Целью настоящего исследования явилось изучение хондропротекторных свойств пептида с условным названием IPH AЕN в культурах хрящевой ткани крысы. Для достижения цели были поставлены следующие задачи:
- Оценить влияние пептида IPH AЕN на экспрессию маркера пролиферации Ki67 и маркера апоптоза p53 в «молодых» и «старых» культурах хондроцитов крысы.
- Изучить влияние пептида IPH AЕN на экспрессию маркера ремоделирования межклеточного матрикса и функциональной активности хондроцитов ММР13 в «молодых» и «старых» культурах хондроцитов крысы.
- Высказать предположение о механизмах хондропротекторного действия пептида IPH AЕN.
2. Материалы и методы исследования
2.1. Характеристика исследуемого материала
Объектами для морфофункционального исследования явились первичные культуры клеток хрящевой ткани молодых крыс линии Вистар. Животных содержали в условиях вивария при комнатной температуре с 12-часовым циклом свет/темнота, свободным доступом к воде и пище, на стандартной диете в соответствии с нормами содержания лабораторных животных.
В работе были исследованы диссоциированные культуры клеток хрящевой ткани крыс линии Вистар, 3 и 14 пассажи: 1- контроль (без добавления пептидов), 2 – добавление пептида IPH AVN в концентрации 20 нг/мл, 3 – добавление пептида IPH AЕN в концентрации 20 нг/мл. Таким образом, для изучения хондропротекторных свойств пептида с условным названием IPH AЕN отрицательным контролем служил пептид IPH AVN. Для большинства диссоциированных клеточных культур, как было показано ранее, наиболее эффективной является концентрация пептидов 20 нг/мл (Линькова Н.С. и др., 2016; Khavinson V. et al., 2017). Поскольку ранее пептид IPH AЕN в диссоциированных культурах клеток не изучали, выбрали концентрацию 20 нг/мл, исходя из данных литературы.
Культивирование проводили до 3 пассажа и до 14 пассажа, на которых клетки были рассеяны на планшеты, и было произведено иммуноцитохимическое окрашивание. 3 пассаж расценивали как «молодые» культуры, а 14 пассаж – как «старые» культуры в соответствии с моделью клеточного старения пассажами.
Еще с 80-ых годов ХХ в. для исследования геропротекторных веществ используется две модели клеточного старения: пассажами и стационарного старения путем контактного торможения (Чирикова Е.Ю. и др., 1984). Границы и условия применимости этих моделей постоянно обсуждаются и в современной литературе (Хохлов А.Н., 2009; 2013; Хохлов А.Н. и др., 2014). Это связано с тем, что в работе с каждой культурой клеток приходится на основе общих рекомендаций подбирать индивидуальные условия культивирования и клеточного старения. Такое предварительное исследование, направленное на соблюдение общих рекомендаций и создания оптимальных условий старения первичной культуры хондроцитов крысы, было проведено и в нашей работе.
2.2.Приготовление раствора пептидов для добавления в культуры клеток
Для исследования использовали пептиды IPH AVN и IPH AЕN в форме лиофилизированного порошка. Осуществляли последовательное разведение пептидов питательной средой для культивирования клеток до получения конечной концентрации раствора 20 нг/мл.
2.3. Выделение первичных культур эндотелиоцитов и хондроцитов крыс
Культуры эндотелия получали из аорты, а культуры хондроцитов – из хрящевой ткани задних конечностей крыс линии Вистар. Изолированную ткань сосуда или хряща измельчали и помещали в 0,2% раствор коллагеназы NB4 (Serva) в течение 30 мин при температуре 37 °С. Полученные клетки высаживали на культуральный пластик без подложки в ростовой среде DMEM/F12 (Invitrogen) с добавлением 10% фетальной бычьей сыворотки (foetal bovine serum, FBS; Autogene Bioclear), 100 Ед/мл пенициллина (Gibco), 100 Ед/мл стрептомицина (Gibco), 2 ммоль/л L-глутамина (Invitrogen). Смену среды проводили каждые трое суток. Для культивирования использовали среду DMEM/F12 (Invitrogen) с добавлением 10% FBS (Autogene Bioclear), 100 Ед/мл пенициллина (Gibco), 100 Ед/мл стрептомицина (Gibco), 2 ммоль/л L-глутамина (Invitrogen). Смену среды проводили каждые трое суток. Общий вид культур эндотелиоцитов и хондроцитов крысы представлен на рисунках 1 и 2.
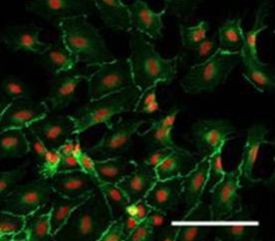
Рис. 1. Первичная культура эндотелиоцитов. Иммунофлуоресцентная конфокальная микроскопия. Из материалов статьи Kuosmanen S.M. et al., 2017.
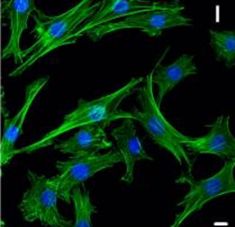
Рис. 2. Первичная культура хондроцитов. Иммунофлуоресцентная конфокальная микроскопия. Масштаб – 10 мкм. Зеленая флуоресценция – актиновый цитоскелет клеток, краситель Alexa Fluor 488. Синим флуоресцируют ядра, краситель DAPI. Из материалов статьи Mellor F.L. et al., 2014.
2.4. Иммунофлуоресцентная конфокальная микроскопия
Для иммуноцитохимического исследования хондроцитов крыс использовали антитела к Ki67 и р53 и маркер ремоделирования межклеточного матрикса и функциональной активности хондроцитов ММР13 (разведение 1:120, Abcam, Англия).
Указанные молекулы были выбраны для исследования, так как они играют важную роль в функционировании и старении хондроцитов. Белок Ki67 является общепризнанным и широко используемым маркером пролиферации. Процесс старения характеризуется достижением предела Хейфлика и снижением либо полным прекращением способности клеток к делению. В связи с этим белок Ki67 может являться важным маркером для оценки снижения пролиферативной активности клеток и степени инволютивных процессов в исследуемом органе (Romero Q. et al., 2014).Белок р53 является транскрипционным фактором, выполняющим функцию супрессора образования злокачественных опухолей путем активации апоптоза в тканях организма. Белок р53 активируется при повреждениях ДНК, а также при стимулах, которые могут привести к подобным повреждениям, или являются сигналом о старении клетки и нарушении ее функциональной активности (Arshad H., et al., 2010). Матриксные металлопротеиназы (ММР), относящиеся к семейству цинковых металлопротеиназ, участвуют в обмене белков межклеточного матрикса. Ведущая роль в процессе физиологического ремоделирования гиалинового хряща сустава отведена металлопротеиназам, относящимся к классу коллагеназ (ММР-1, ММР-13 и др.). В норме металлопротеиназы секретируются фибробластами, хондроцитами, эпителиальными клетками, макрофагами в очень малых количествах в неактивном состоянии. Важной особенностью металлопротеиназ является их способность к индукции под действием различных факторов. Регуляция активности коллагеназ осуществляется цитокинами, факторами роста, различными химическими соединениями (липополисахариды бактериального происхождения и др.), факторами, влияющими на мембрану клетки. Активность ММР подавляется тканевыми ингибиторами металлопротеиназ (TIMP), а также гормонами (глюкокортикостероиды и т.п.). Ранее считалось, что главная роль в деструкции матрикса принадлежит ММР-1, затем была установлена и важная роль ММР-13, которая разрушает коллаген II типа, стромелизин и др. Известно, что в механизмах активизации металлопротеиназ значимую роль отводят сигнальным белкам S100A8 и A9. В результате, активируются NF-kB рецепторы синовиальных фибробластов, что определяет высвобождение многих цитокинов, таких как ИЛ-6, ИЛ-10, GM-CSF, IL-8 и хемоаттрактант моноцитов, который, в свою очередь, играет значимую роль в активации металлопротеиназ и обуславливает их высокую активность при остеоартрозе (Демкин С.А. и др., 2017).
Окрашивание препаратов проводили по стандартному протоколу:
- Промывка клеточной культуры раствором PBS.
- Фиксация клеток: для фиксации используется 4% раствор параформальдегида на PBS (инкубация в течение 15 минут при комнатной температуре).
- Промывка раствором PBS (три смены по 3 минуты).
- Отмывка дистиллированной водой (3 минуты).
- Пермеабилизация клеток осуществляется 0,25-0,5% раствором Triton X-100 на PBS (Биолот, РФ) в течение 15 минут при комнатной температуре.
- Промывка в трех сменах PBS (по 3 минуты).
- Инкубация в 1% бычьем сывороточном альбумине, разведенным PBS, pH 7,5 в течение 15 минут для блокировки неспецифического связывания.
- Промывка в трех сменах PBS (по 3 минуты).
- Инкубация с первичными антителами (время и условия инкубации установлены производителем в инструкции к антителам).
- Промывка в трех сменах PBS (по 3 минуты).
- Инкубация со вторичными антителами, конъюгированными с флуорохромом Alexa Fluor 488 или Alexa Fluor 647, в течение 30 минут при комнатной температуре в темноте.
- Промывка в трех сменах PBS (по 3 минуты).
- Готовые препараты заключить под покровные стекла в монтирующую среду Dako Fluorescent Mounting Medium (Dako, США) и хранить в темноте, во избежание быстрого выгорания флуорохрома.
2.5. Морфометрия

Для анализа полученных результатов использовали конфокальный микроскоп Olympus FluoView 1000 (Япония), программное обеспечение «Olympus FluoView ver 3.1b». В каждом случае анализировали 10 полей зрения при увеличении ×200. Проводили измерение относительной площади экспрессии в %. Относительную площадь экспрессии рассчитывали, как отношение площади, занимаемой иммунопозитивными клетками, к общей площади клеток в поле зрения и выражали в процентах для маркера с цитоплазматическим окрашиванием (MMP13), а также как отношение площади, занимаемой иммунопозитивными ядрами, к общей площади ядер в поле зрения для маркеров с ядерной экспрессией (р53, Ki67)
2.6. Статистическая обработка результатов
Статистическая обработка экспериментальных данных включала в себя подсчет среднего арифметического, стандартного отклонения и доверительного интервала для каждой выборки и проводилась в программе Statistica 6.0. Для анализа вида распределения использовали критерий Шапиро-Уилка (Shapiro-Wilk’s W-test). Если данные подчинялись нормальному распределению, различия в средних определялись с помощью критерия Стюдента (t). В случаях, когда дисперсионный анализ выявлял статистически значимую неоднородность нескольких выборок, для последующего выявления неоднородных групп (путем их попарных сравнений) применяли процедуры множественных сравнений с помощью
U-критерия Манна-Уитни. Критический уровень достоверности нулевой гипотезы (об отсутствии различий) принимали равным 0,05.
3. Результаты исследования и их обсуждение
3.1. Влияние пептида IPH AЕNна экспрессию Ki67 и р53 в «молодых» и «старых» культурах хондроцитов крысы
Иммунофлуоресцентным методом было показано, что площадь экспрессии Ki67 в контроле «молодых» культур составила (2,8±0,3)%, что достоверно в 1,8 раза больше, чем в «старых культурах» — (1,6±0,1)%. Под действием пептида IPH AЕN происходило достоверное увеличение экспрессии Ki67 в «старых» культурах в 2 раза (рис. 3).
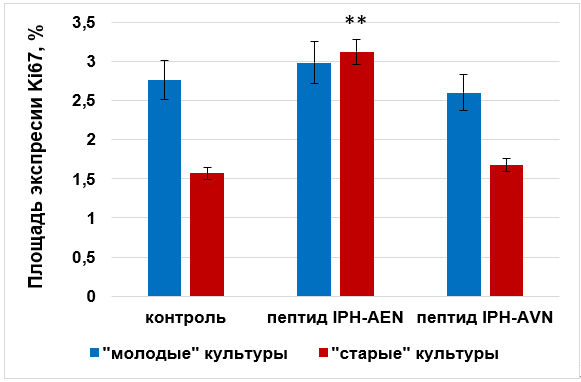
Рис. 3. Влияние пептидов на экспрессию Ki67 в культуре хондроцитов крысы. * — р <0,05 по сравнению с контрольной группой «молодые» культуры; ** — р <0,05 по сравнению с контрольной группой «старые» культуры.
В «молодых» культурах пептид IPH AЕN достоверно не влиял на экспрессию Ki67. Пептид IPH AVN не оказывал влияния на экспрессию Ki67 в культурах хондроцитов (рис. 3).
Иммунофлуоресцентным методом было показано, что площадь экспрессии р53 в контроле «молодых» культур составила (0,8±0,1)%, что достоверно в 4,6 раза ниже, чем в «старых» культурах — (3,7±0,6)%. Под действием пептида IPH AЕN происходило достоверное снижение экспрессии р53 в «молодых» и «старых» культурах соответственно в 1,8 и 2,1 раза (рис. 4). Под влиянием пептида IPH AVN происходило достоверное повышение экспрессии р53 в «молодых» культурах хондроцитов в 1,5 раза. При этом пептид IPH AVN не влиял на исследуемый показатель в «старых» культурах (рис. 4).
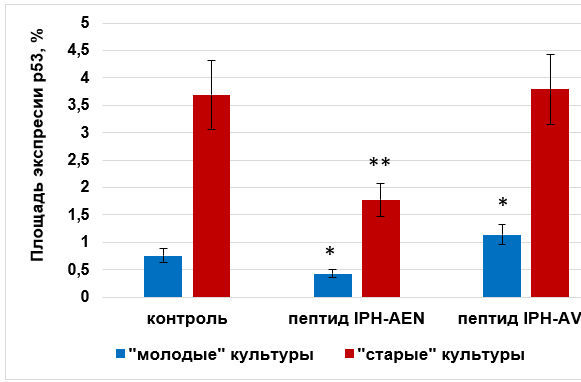
Рис. 4. Влияние пептидов на экспрессию р53 в культуре хондроцитов крысы. * — р <0,05 по сравнению с контрольной группой «молодые» культуры;
** — р <0,05 по сравнению с контрольной группой «старые» культуры.
3.2. Влияние пептида IPH AЕN на экспрессию ММР13 в «молодых» и «старых» культурах хондроцитов крысы
Иммунофлуоресцентным методом было показано, что площадь экспрессии ММР13 в контроле «молодых» культур составила (0,3±0,05)%, что достоверно в 13 раз ниже, чем в «старых» культурах — (3,9±0,7)%. Под действием пептида IPH AЕN происходило достоверное снижение экспрессии ММР13 в «старых» культурах в 2,7 раза (рис. 5). Пептид IPH AЕN не влиял на экспрессию ММР13 в «молодых» культурах хондроцитов. Пептид IPH AVN не влиял на исследуемый показатель в «молодых» и «старых» культурах хондроцитов (рис. 5).
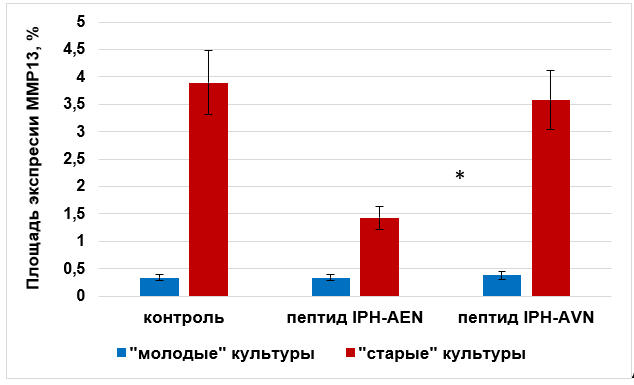
Рис. 5. Влияние пептидов на экспрессию ММР13 в культуре хондроцитов крысы. * — р <0,05 по сравнению с контрольной группой «старые» культуры.
Данные о влиянии пептида IPH AЕN на экспрессию белков Ki67, p53, ММР13 в культурах хондроцитов при их старении могут играть важную роль в понимании молекулярных механизмов действия этого пептида при дегенеративных процессах в хрящевой ткани суставов. Известно, что с возрастом процессы апоптоза (экспрессия транскрипционного фактора р53) начинают преобладать над процессами пролиферации (экспрессия Ki67). Это является одним из факторов развития патологии опорно-двигательного аппарата при старении и у лиц молодого и среднего возраста, подвергающихся интенсивным физическим нагрузкам. Ту же тенденцию мы наблюдаем и при старении хондроцитов в культуре. Пептид IPH AЕN стимулирует пролиферацию хондроцитов и снижает выраженность апоптоза, особенно в условиях клеточного старения. Кроме того, пептид IPH AЕN снижает выраженность экспрессии белка, участвующего в ремоделировании межклеточного матрикса, ММР13, характерного для воспалительных заболеваний хрящевой ткани. Таким образом, пептид IPH AЕN может рассматриваться как вещество, потенциально перспективное для исследований в качестве эффективного хондропротекторного средства.
ВЫВОДЫ
-
При старении хондроцитов в культуре экспрессия Ki67 снижается в 1,8 раза. Пептид IPH AЕN повышает экспрессию пролиферотропного белка Ki67 в «старых» культурах хондроцитов крысы соответственно в 2 раза. При старении хондроцитов в культуре экспрессия р53 повышается в 4,6 раза. Пептид IPH-AEN снижает экспрессию р53 «молодых» и «старых» культурах клеток соответственно в 1,8 и 2,1 раза.
-
При старении хондроцитов в культуре экспрессия маркера ремоделирования межклеточного матрикса ММР13 возрастает в 13 раз. Под действием пептида IPH AЕN происходит снижение экспрессии ММР13 в «старых» культурах в 2,7 раза.
-
Стимуляция пролиферации (экспрессия белка Ki67), снижение выраженности апоптоза (белок р53) и ремоделирования межклеточного матрикса (экспрессия ММР13) под действием пептида IPH AЕN могут указывать на способность этого пептида предотвращать развитие дегенеративных процессов в хрящевой ткани суставов.
Литература
- Алексеева Л.И. Препараты замедленного действия в лечении остеоартроза // РМЖ. — 2012. — № 7. — С. 389–393.
- Балабанова Р.М. Новый подход к лечению остеоартроза как хронического воспалительного заболевания // Современная ревматология. — 2013. — № 2. — С. 95–98.
- Башкирёва А.С., Артамонова В.Г. Пептидергическая коррекция невротических состояний у водителей грузового автотранспорта// Успехи геронтологии. — 2012. — Т. 25. — № 4. — С. 718-728.
- Владимирская Т.Э., Швед И.А., Криворот С.Г. Апоптоз клеток стенки коронарных артерий как фактор развития и прогрессирования коронаросклероза // Актуальные вопросы кардиологии. — 2013. — N 9. — P. 22–26.
- Гаврилова Н.Е., Метельская В.А., Перова Н.В., Яровая Е.Б., Мазаев В.П., Уразалина С.Ж., Бойцов С.А. Взаимосвязь между выраженностью коронарного атеросклероза, факторами риска и маркерами атеросклеротического поражения каротидных и периферических артерий // Кардиоваскулярная терапия и профилактика. – 2013. – Т. 12. – № 1. – С. 40–45.
- Демкин С.А., Маланин Д.А., Рогова Л.Н., Снигур Г.Л., Григорьева Н.В., Байдова К.В. Металлопротеиназы 1 и 13 как маркеры деструктивно-пролиферативного процесс суставного хряща при экспериментальном остеоартрозе // Вестник Волг ГМУ. – 2017. – Вып. 1 (61). – С. 69-73.
- Линькова Н.С., Дробинцева А.О., Орлова О.А., Кузнецова Е.П., Полякова В.О., Кветной И.М., Хавинсон В.Х. Пептидная регуляция функций фибробластов кожи при их старении in vitro // Клеточные технологии в биологии и медицине. – 2016. — №1. – С. 40-44.
- Олюнин Ю.А. Остеоартроз коленных суставов. Особенности диагностики и современные принципы лечения // РМЖ. — 2015. — №7. — С. 404.
- Струков В.И., Джоунс О.В., Крутяков Е.Н. Способ диагностики остеопороза методом определения динамики закрытия полостных образований для оценки эффективности применения различных остеопротекторов// Патент на изобретение №2511430. Приоритет с 19.04.2012.
- Хохлов А.Н. Тестирование геропротекторов в экспериментах на клеточных культурах: за и против // Проблемы старения и долголетия. — 2009. — Т. 18. — № 1. — С. 3236.
- Хохлов А.Н. Эволюция термина «cellular senescence» и ее влияние на состояние современных цитогеронтологических исследований // Вестник Московского университета. Серия 16: Биология. — 2013. — №4. — С. 18-22.
- Хохлов А.Н., Клебанов А.А., Кармушаков А.Ф., Шиловский Г.А., Насонов М.М., Моргунова Г.В. Тестирование геропротекторов в экспериментах на клеточных культурах: выбор оптимальной модельной системы // Вестник Московского университета. Серия 16: Биология. — 2014. — №1. — С. 13-18.
- Arshad H., Ahmad Z., Hasan S.H. Gliomas: correlation of histologic grade, Ki67 and p53 expression with patient survival // Asian Pac J Cancer Prev. – 2010. – Vol. 11. – N 6. – P. 1637-1640.
- Khavinson V., Linkova N., Kukanova E., Bolshakova A., Gainullina A., Tendler S., Morozova E., Tarnovskaya S., Vinski D.S.P., Bakulev V., Kasyanenko N. Neuroprotective Effect of EDR Peptide in Mouse Model of Huntington’s Disease // J. of Neurology and Neuroscience. – 2017. — Vol.8. — No.1:166. – P. 1-11.
- Kuosmanen S.M., Kansanen E., Sihvola V., Levonen A.-L. MicroRNA Profiling Reveals Distinct Profiles for Tissue-Derived and Cultured Endothelial Cells// Sci Rep. 2017. Vol. 7. P. 10943.
- Kvetnoy I.M., Paltsev M.A., Polyakova V.O. et al. Tau-Protein Expression in Human Buccal Epithelium: A Promising Non-Invasive Marker for Life-Time Diagnosis of Alzheimer’s Disease // Journal of Advanced Biomarkers Research. – 2015. – N1. – P. 1-6.
- Mellor F.L., Baker T.L., Brown R.J., Catlin L.W., Oxford J.T. Optimal 3-D culture of primary articular chondrocytes for use in the Rotating Wall Vessel Bioreactor// Aviat Space Environ Med. – 2014. – Vol. 85, N 8. P. 798–804.
- Orekhov A.N., Andreeva E.R., Bobryshev Y.V. Cellular mechanisms of human atherosclerosis: Role of cell-to-cell communications in subendothelial cell functions // Tissue Cell. — 2016. — V. 48. — N 1. — P. 25-34.
- Pfenniger A., Chanson M., Kwak B.R. Connexins in atherosclerosis. // Biochim Biophys Acta. – 2013. – Vol. 1828 – N 1. – P. 157–166;
- Romero Q., Bendahl P.O., Ferno M. et al. A novel model for Ki67 assessment in breast cancer. // Diagn Pathol. – 2014. – Vol. 16. – N 9. – P. 118.
- Wang M., Jiang L., Monticone R.E., Lakatta E.G. Proinflammation: the key to arterial aging. // Trends Endocrinol. Metab. – 2014. – Vol. 25. N 2. – P. 72–79.
- Yano Y., Ning H., Allen N., Reis J.P., Launer L.J., Liu K., Yaffe K., Greenland P., Lloyd–Jones D.M. Long–Term Blood Pressure Variability Throughout Young Adulthood and Cognitive Function in Midlife: The Coronary Artery Risk Development in Young Adults (CARDIA) Study. // Hypertension. – 2014. – P. 983-989.




